Batérie sa vyvíjajú nielen revolučnými skokmi, ale vylepšuje ich aj technologická evolúcia, hoci to nijako výrazne nevnímame. Za 20 rokov od roku 1994 sa napríklad energetická hustota „tých istých“ Li-ion batérií zvýšila trojnásobne. Boom prenosnej elektroniky, ale najmä začínajúca éra elektromobilov si však žiada skutočnú revolúciu.
V pátraní po menších, silnejších a trvanlivejších batériách by sa takýmto riešením mohla stať technológia lítium – vzduch (Li-air, niekde označovaná aj ako Li-O2). Hovorí sa, že prvé akumulátory Li-air boli objavené vďaka náhode, keď pri testovaní Li-ion batérií v roku 1995 do nich vnikol vďaka netesnosti vzduch a články vykazovali vyššiu hustotu energie. Zatiaľ tento objav neviedol k vývoju technicky konkurencieschopných batérií, ale môže to zmeniť výskum vedcov z University of Cambridge, ktorého výsledky publikoval magazín Science.
Výskum pod vedením profesorov Gunwoo Kima a Clare Greya pracuje s Li-air bunkami, ktoré používajú vodič elektrónov z ľahkého, pórovitého uhlíka, namiesto v Li-ion batériách bežne používaných kovových oxidov. Tým sa ušetrí na hmotnosti, ale prináša to aj vlastné problémy.
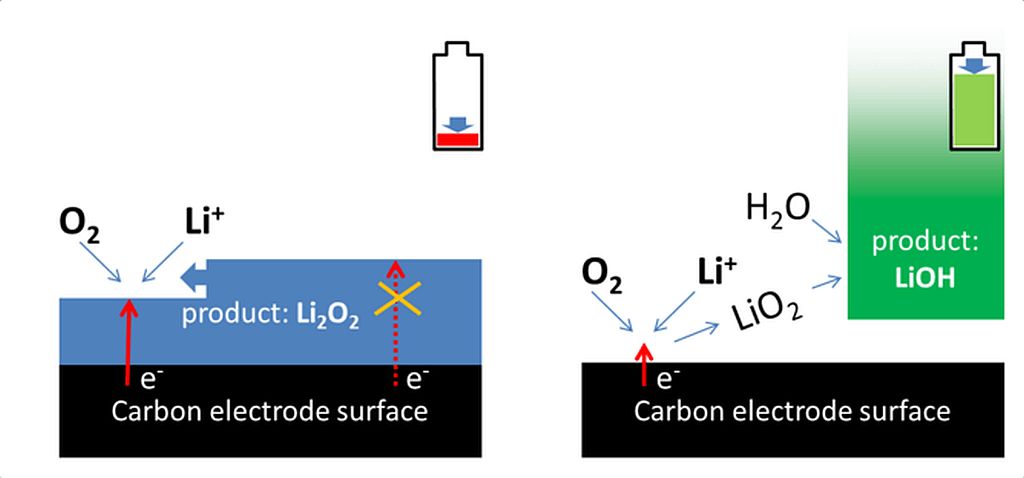
Li-air batérie s peroxidom lítia (vľavo, blokovanie uhlíkovej elektródy) a hydroxidom lítnym (vpravo, s odblokovanou elektródou) počas vybíjania. Pórovitá štruktúra elektródy nie je pre jednoduchosť zobrazená.
Li-air batéria vytvára napätie za prítomnosti molekúl kyslíka (O2) na kladnej elektróde. O2 reaguje s kladne nabitými iónmi lítia, vytvorí peroxid lítia (Li2O2) a generuje elektrickú energiu. Elektróny sú odvádzané z elektródy a batéria je vybitá, ak už nemôže vytvárať ďalší Li2O2.
Ale Li2O2 je veľmi zlým vodičom elektrónov. Ak sa na povrchu elektródy, ktorá dodáva elektróny pre reakciu, vytvárajú ložiská Li2O2, tlmí to, a nakoniec zastaví reakciu, a tým aj energiu batérie. Tento problém možno prekonať tak, že reakčný produkt (v tomto prípade peroxid lítia) je uložený v blízkosti elektródy, ale netvorí povlak na jej povrchu.
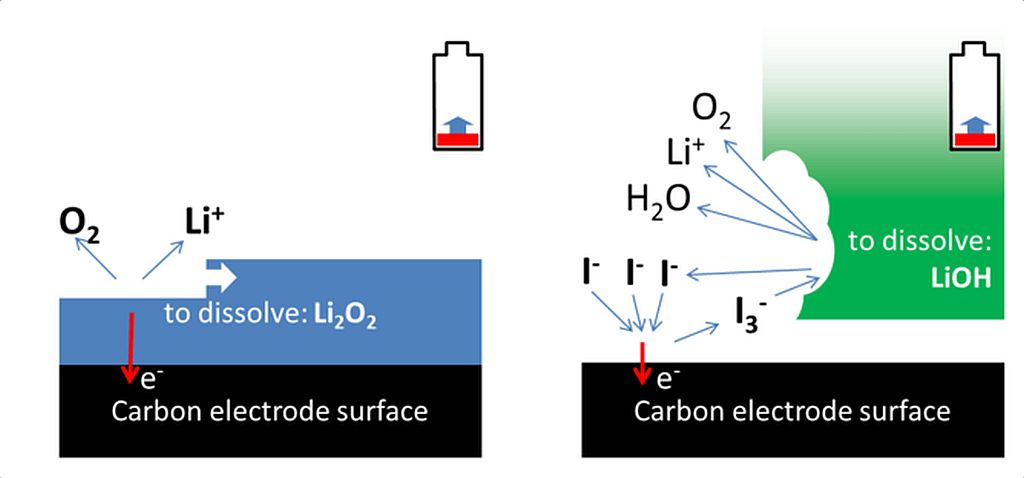
Nabíjanie Li-air batérie. Vľavo: peroxid lítia musí byť odstránený z povrchu uhlíka. Vpravo: cyklus jodidu a trijodidu, kde trijodid chemicky rozpúšťa hydroxid lítny, uvoľňuje prvky, takže môžu byť znovu rekombinované pre výrobu elektrickej energie.
Výskumníci z Cambridge našli metódu, ako to urobiť – do štandardného elektrolytu pridali ako prísadu jodid lítny (LI). Experiment tiež zahŕňa poréznu, nadýchanú elektródu vyrobenú z mnohých tenkých vrstiev grafénu s veľkými pórmi. Poslednou dôležitou zložkou je malé množstvo vody.
S touto kombináciou chemických látok vzniká reakcia, ktorá pri vybíjaní netvorí Li2O2, ktorý by odstavil vodivý povrch elektródy, ale miesto toho použije vodík extrahovaný z vody na vytvorenie krištáľov hydroxidu lítneho (LiOH). Tieto kryštály vyplnia veľké póry v „nadýchanej“ uhlíkovej elektróde, ale zásadným spôsobom neblokujú povrch uhlíka, ktorý je zdrojom napätia. Takže prítomnosť jodidu lítneho ako „pomocníka“ (hoci jeho presná úloha zatiaľ nie je jasná) a vody ako koreaktantu v tomto procese zvyšuje kapacitu batérie Li-air.
Nové batérie by mali mať údajne až 10x vyššiu kapacitu (objemovú energetickú hustotu) oproti bežným Li-ion batériám a to pri pätinovej hmotnosti. To sú parametre o akých výrobcovia elektromobilov, ale aj laptotpov a ďalších zariadení snívajú. Náklady na výrobu by mali byť tiež podstatne (až 5x) nižšie. Nepríjemnou, ale nie neočakávanou správou je, že komerčná dostupnosť nových batérií nie je zatiaľ na dosah. Sériovej výrobe má predchádzať ešte niekoľkoročný vývoj, ale aspoň môžeme nahliadnuť na horizont budúcich možností, ktoré vyzerajú nádejne.

